【醫學新觀點】十二指腸空腸套管術對肥胖糖尿病患者內分泌激素的影響
引言:
作為人體最大的內分泌器官,胃腸道在血糖穩態調控和糖尿病治療中的作用日益凸顯。腸道產生的胰高糖素原衍生肽(PGDPs),即胰高糖素樣肽-1(GLP-1)、GLP-2、胃抑制多肽(GIP)、胃泌酸調節素、腸高血糖素等,通過多條途徑參與機體血糖穩態調節。近年來,基于腸道PGDPs的療法、藥物能夠糾正肥胖糖尿病發病機制中的多種病理生理缺陷,有效改善血糖,已成為糖尿病領域的研究熱點。
研究發現,代謝手術在導致體重下降的同時也會影響胰島內各種內分泌激素的合成與分泌,進而調控糖代謝過程[1]。十二指腸空腸套管術(DJBS)作為借鑒了代謝手術Roux-en-Y胃旁路術式(RYGB)手術原理的新興療法,推測其也有類似機制。本文筆者將對DJBS對肥胖糖尿病患者內分泌激素水平的影響進行綜述,以進一步梳理其降糖機制,為糖尿病的治療提供新思路。
正文:
肥胖及糖尿病目前已成為全世界范圍的公共健康問題,嚴重影響患者的健康并加劇家庭生活的負擔,而代謝手術已經在病態肥胖和肥胖糖尿病及其他代謝異常的治療方面發揮出了明顯優勢。隨著證據的不斷積累,代謝手術已成為目前具有充足證據支持、可長期緩解糖尿病的治療方法[2]。在目前已經開展的各種代謝手術患者身上,我們觀察到了患者術前術后內分泌激素的顯著變化,而這些內分泌激素的變化,可能是產生相關療效的重要機制。
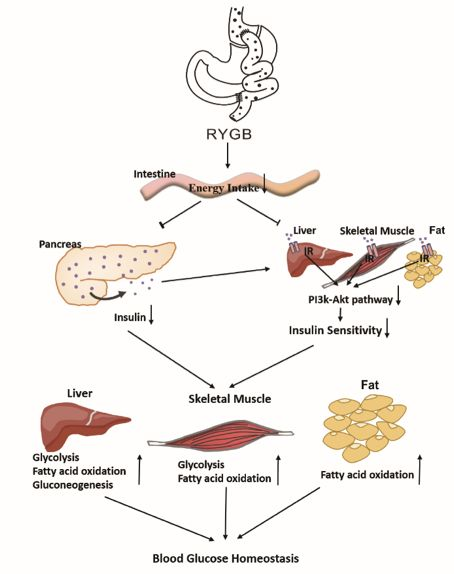
以代謝手術“金標準”——RYGB術舉例,其通過曠置胃、十二指腸和部分空腸,減少了腸道的能量攝入,使胰島素的合成和分泌減少,而胰島素敏感組織對胰島素敏感性下降,使組織的非胰島素依賴通路的激活,促進糖酵解和脂肪酸氧化,從而維持血糖穩態(圖1)。在其他大量代謝性手術的研究中,研究者發現部分患者RYGB術后甚至可以達到糖尿病的完全緩解,而且這種緩解效果甚至獨立于體重減輕[3]。雖然RYGB是治療肥胖和2型糖尿病有效且持久的方法,但其局限性包括圍手術期并發癥的風險以及其人體結構改變的不可逆轉性等,致使其風險收益比和患者接受度普遍偏低。因此,醫學界已經做出了相當大的努力來研發可逆且侵入性較小的方法,用以模擬RYGB的效果。
作為 RYGB 的替代療法,DJBS 借鑒了 RYGB 的手術原理,通過胃鏡在十二指腸及空腸上段置入一個套管,以隔絕十二指腸和空腸近端食糜與腸壁的接觸,減少營養吸收,從而達到治療目的。不同的是,DJBS 規避了RYGB術帶來的永久性生理結構破壞損失、手術并發癥等風險,是一種可逆的方法[4],這也為肥胖及糖尿病治療提供了全新的治療方法和理念。那么,DJBS是否也跟RYGB一樣影響著患者的內分泌激素水平呢?
由于兩者同原,故筆者猜測其很多療效機制可能與 RYGB 相同或類似。在捷克進行的一項“肥胖2型糖尿病患者十二指腸空腸隔絕術的內分泌影響”的臨床試驗中[5],研究者篩選了30名血糖控制不佳的肥胖2型糖尿病患者接受DJBS術,在術前及術后的第1、第6、第10個月評估其人體測量參數、血糖控制、代謝和激素譜。結果發現,DJBS術置入后患者減輕了體重(表1),改善了血脂水平和血糖控制,同時降低了血糖波動性。成纖維細胞生長因子19(FGF19)和膽汁酸的血清濃度顯著增加,并有恢復餐后GLP-1峰值的趨勢。在取出DJBS套管后3個月,體重下降和血糖控制改善的療效持續存在(圖2)。因此,研究團隊得出結論,DJBS的置入可以保持體重的持續減輕以及血脂和血糖控制的改善,而FGF19和膽汁酸水平的增加可能是這些效應的部分原因。研究者還發現患者各項血糖監測指標,在DJBS置入后1周即有明顯的改善,且改善效果早于患者體質量的變化,這也與RYGB術的研究結果類似[6]。

表1 DJBS治療不同階段身體測量參數及生化指標
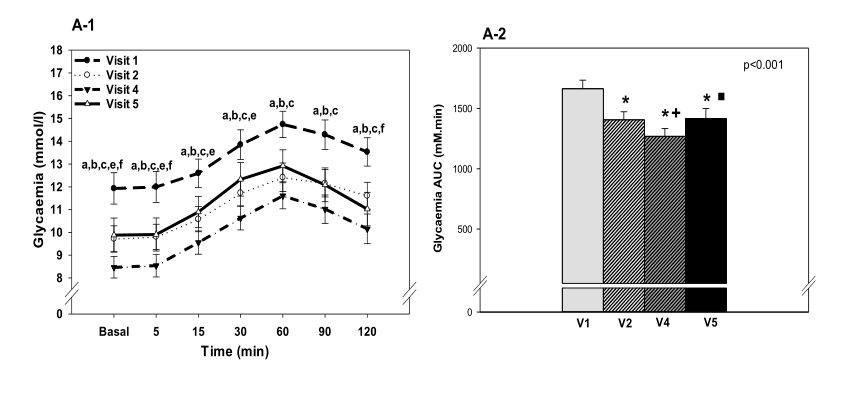

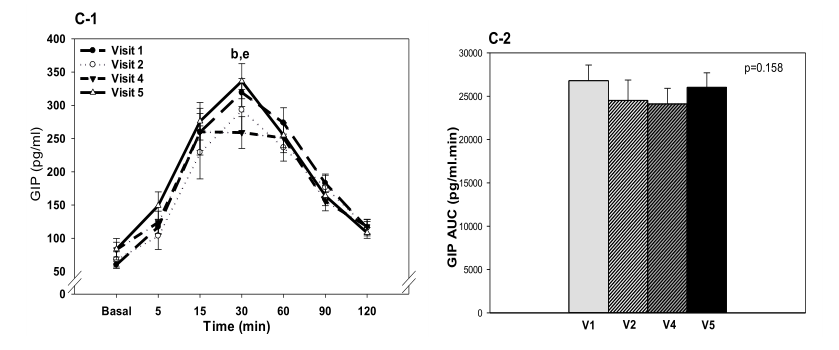

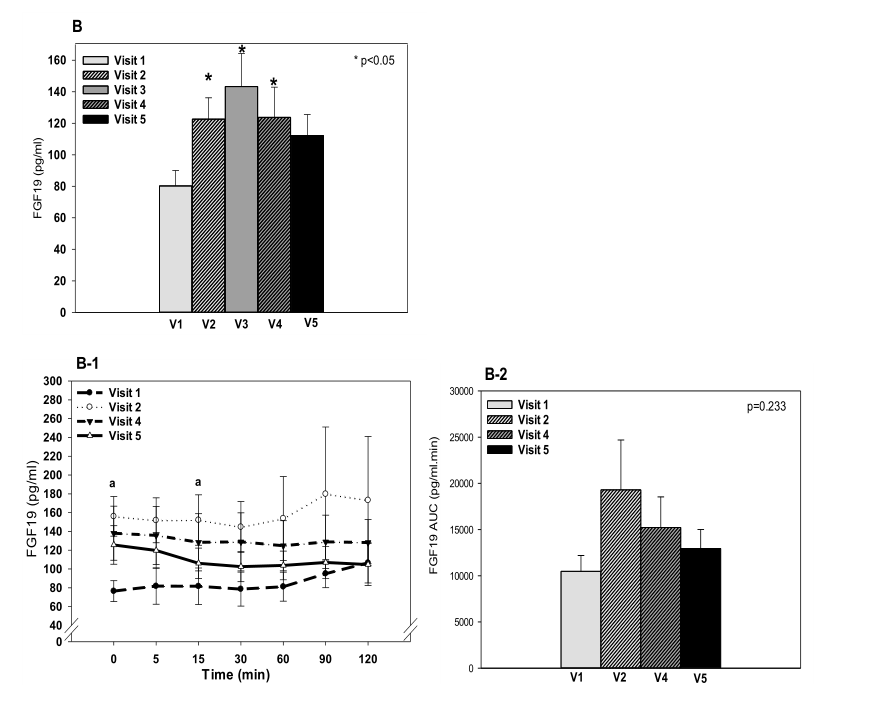
圖2 DJBS治療不同階段血糖和內分泌激素變化
從上述的研究結果來看,DJBS可以通過影響患者內分泌激素水平的類似機制來降低血糖,而類似的研究結論也在中國得到了驗證。在最近一項來自于浙江杭州的研究中,患者(年齡:35.2±7.2 歲;61.5% 的女性)使用了國內科研型企業自主研發的“胃轉流支架系統”(TONGEE? DJBS)進行了 3 個月的置入治療。3個月后,患者減重效果顯著(BMI-4.3kg/m2,95%CI?4.9至?3.7),且患者的肝脂肪變性、肝酶、胰島素抵抗和代謝參數(HbA1c -6.3±1.7%比5.6±0.6%,P<0.05)(表 2)同樣得到了明顯改善[7]。

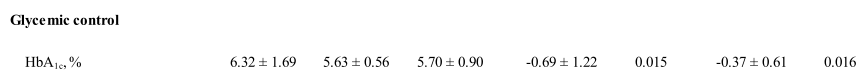
表2 TONGEE DJBS 植入后 HbA1c 變化
對于未來的展望,筆者認為,“胃轉流支架系統”這類內鏡治療手段已經在緩解肥胖、2型糖尿病等代謝性疾病領域上顯示出了獨特優勢,其后續的正式臨床應用也十分令人期待。相信隨著規范化研究證據的不斷完善,該類技術有望成為治療糖尿病的新選擇,讓更多的患者從中獲益。后續筆者也將繼續關注此類新技術的臨床研究及學術內容。
參考文獻:
[1] 佚名.Metabolic improvements following Roux-en-Y surgery assessed by solid meal test in subjects with short duration type 2 diabetes.[J].BMC obesity.2017.41-9.DOI:10.1186/s40608-017-0149-1.
[2] CarlssonL, Sj?holmK, JacobsonP, et al. life expectancy after bariatric surgery in the Swedish obese subjects study[J]. N Engl J Med, 2020, 383(16):1535-1543. DOI: 10.1056/NEJMoa2002449.
[3] Cummings DE 2009 Endocrine mechanisms mediating remission of diabetes after gastric bypass surgery. Int J Obes (Lond) 33 Suppl 1 S33-40.
[4] Patel SR, Mason J & Hakim N 2012 The Duodenal-Jejunal Bypass Sleeve (EndoBarrier Gastrointestinal Liner) for Weight Loss and Treatment of Type II Diabetes. Indian J Surg 74 275-277.
[5] Kaválková P, Mráz M, Trachta P, et al. Endocrine effects of duodenal-jejunal exclusion in obese patients with type 2 diabetes mellitus. J Endocrinol. 2016;231(1):11-22.
[6] O'Brien PaulE,Dixon JohnB.Health outcomes of severely obese type 2 diabetic subjects 1 year after laparoscopic adjustable gastric banding.[J].Diabetes care.2002,25(2).
[7] Ren M, Zhou X, Yu M, et al. Prospective study of a new endoscopic duodenal-jejunal bypass sleeve in obese patients with nonalcoholic fatty liver disease (with video) [published online ahead of print, 2022 Jul 23]. Dig Endosc. 2022;10.1111/den.14409.



